足球篮球直播平台
>
足球篮球直播平台 > 行业资讯
中药和生物制品注册改革启幕!两意见稿透露未来风向
来源:信息员 点击量:4397 时间:2017-11-13
1月23日,CFDA顺寻公布的《消毒产品注冊维护有效的方法(修编稿)》和《〈中国民众中国消毒产品维护法〉校正案(草案听取看法稿)》的听取看法稿,都会紧扣1月1日中共中央办接待室厅、住建部接待室厅发布《观于推进机构创新审评定批问责制度机构创新激励消毒产品社区医疗仪器创新创新的看法》提交36项重点机构创新错施做的修正。
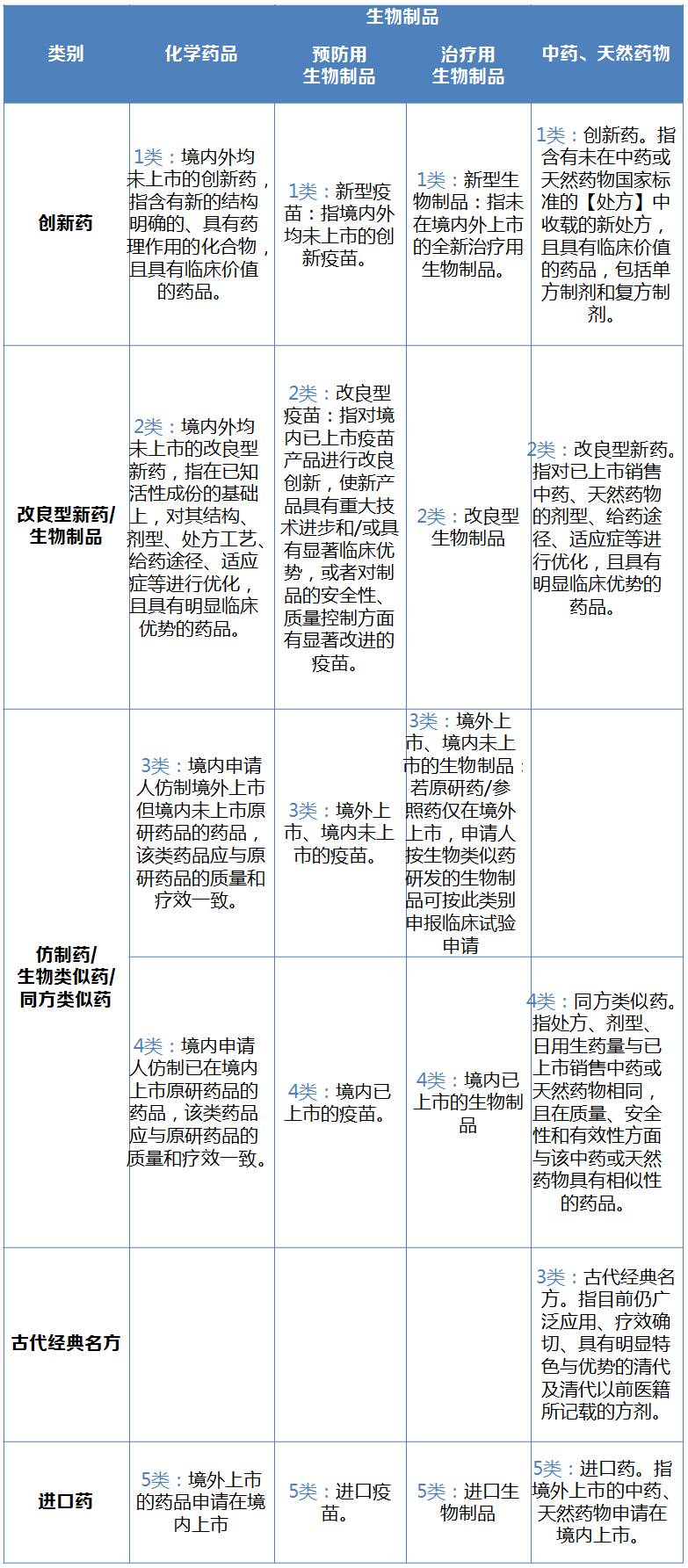
1月23日,CFDA顺寻公布的《消毒产品注冊维护有效的方法(修编稿)》和《〈中国民众中国消毒产品维护法〉校正案(草案听取看法稿)》的听取看法稿,都会紧扣1月1日中共中央办接待室厅、住建部接待室厅发布《观于推进机构创新审评定批问责制度机构创新激励消毒产品社区医疗仪器创新创新的看法》提交36项重点机构创新错施做的修正。
