足球篮球直播平台
>
科技研发 > 研发动态
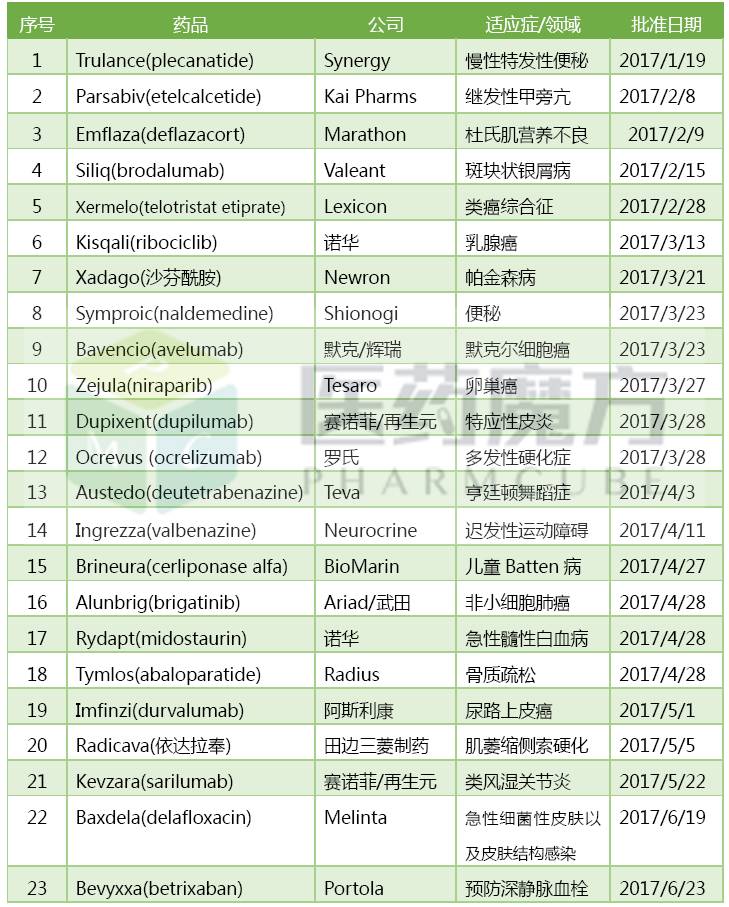
2017上半年FDA批准的新药
来源:医药魔方 点击量:4015 时间:2017-06-29
2017上6个月FDA共核准23个抗癌药物,涉及到16个新大分子片体和五类新生儿物纺织品。这类数字式就可超过二零一六年整年核准的抗癌药物个数求和。近20余载核准抗癌药物个数至多的农历年是206年的4五类,上6个月核准了14个抗癌药物。假若按此市场需求不断发展壮大,2014年核准的抗癌药物个数将破记录发展历史新高度。 2017上几年FDA审批的仿制药